张 荣
本文通信作者,河北医科大学公共卫生学院教授,博士生导师。主要研究领域为环境毒理学、空气污染的健康效应、锂电池金属污染与健康等。
研究背景
随着全球老龄化加剧,寻找影响生物年龄的环境因素成为重要课题。微量元素(铜、锌、铁等)作为"双刃剑"—既是必需营养元素,过量又可能引发毒性效应。越来越多证据表明,微量元素在衰老进程中扮演关键角色,但它们如何通过炎症通路影响生物年龄,以及体育运动能否减轻其不良效应,仍需深入探索。
针对上述问题,河北医科大学公共卫生学院张荣教授团队联合华中科技大学同济医院荆涛教授开展的社区研究,于2025年4月在Journal of Hazardous Materials杂志在线发表了题为Associations between serum trace elements and biological age acceleration in the Chinese elderly: A community-based study investigating the mediating role of inflammatory markers and the moderating effect of physical activity的研究论文,旨在揭示微量元素、炎症、体育运动与生物年龄加速(KDM-BAA)的复杂关联,为 “健康老龄化”提供新视角。

来源:Journal of Hazardous Materials
研究方法
1. 研究人群与检测指标
本研究基于武汉市主城区老年居民多中心健康体检队列,采用横断面研究设计,结合社区流行病学调查与生物标志物检测,探讨中国典型内陆城市老年人群的健康特征。研究对象的纳入需满足两项条件:具有武汉市常住户口,且连续居住时间不少于6个月;65岁及以上。排除标准包括:常规体检中静息心电图检测结果异常者;存在已知职业危害或生活方式相关风险因素暴露史者;过去12个月内报告有创伤性损伤史(含跌倒、滑倒、交通事故、烧伤、穿透伤及中毒);流行病学资料不完整或信息不足以致影响分析者。本研究最终纳入符合标准的受试者共852例。
2. 检测方法
采用电感耦合等离子体质谱仪(ICP-MS)测定铜(Cu)、锌(Zn)、铁(Fe)等7种元素。
生物年龄:通过Klemera-Doubal方法(KDM)计算生物年龄,其与实际年龄回归的残差值即为KDM-BAA。
炎症标记物:检测全身炎症指数(SII)、中性粒细胞-淋巴细胞比值(NLR)等5项指标。
体育运动:按世界卫生组织标准,分为“活跃”(每周≥150 min中等强度运动)和“不活跃”组。
3. 统计方法
单因素分析:广义线性模型(GLM)分析单个微量元素与KDM-BAA的关联。
非线性关系:限制立方样条(RCS)探索剂量-反应曲线。
混合效应:量化-g-计算(Qgcomp),加权分位数回归(WQS),贝叶斯核机器回归(BKMR)评估多种元素联合作用。
机制探索:生信富集分析发现金属和衰老相关的可能通路(炎症通路);中介分析验证炎症标记物的中介作用,有调节的中介分析探讨体育运动在金属→炎症→衰老这个过程的调节作用。
中介分析:探讨炎症因子在环境微量元素暴露与KDM-BAA关联中的潜在中介作用。研究选取中性粒细胞计数(NEU)、NLR、血小板-淋巴细胞比值(PLR)、血小板计数(PLT)及SII作为候选炎症标志物。
调节分析:探讨了体育运动(PA)对环境微量元素、炎症及KDM-BAA关系的调节作用。
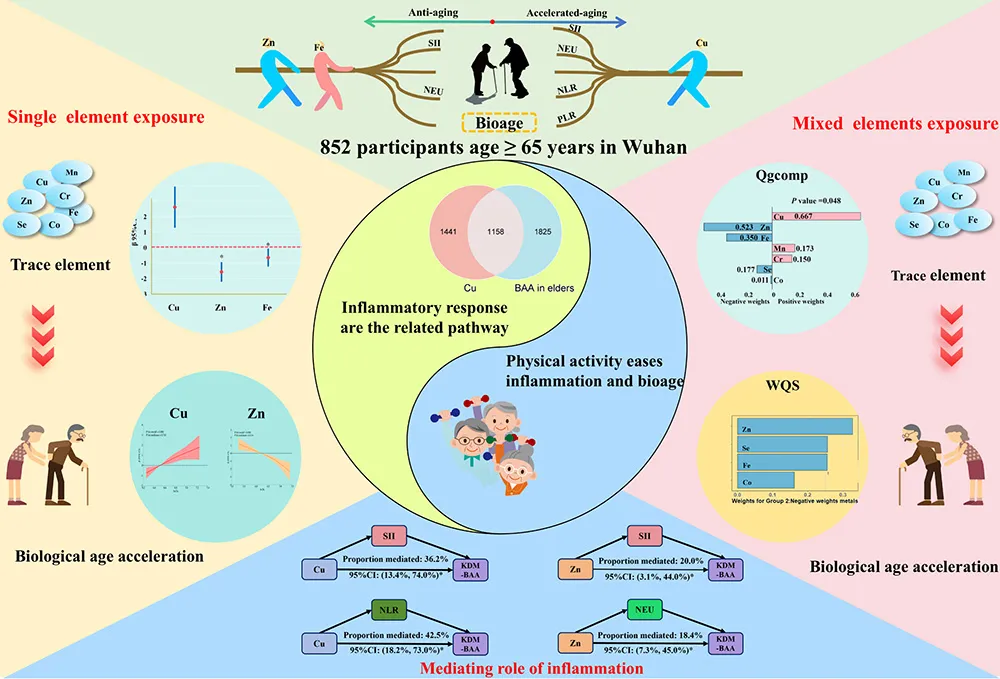
来源:Journal of Hazardous Materials
研究结果
1. 人群基线信息
本研究共纳入852名符合标准的老年受试者(男性313人,女性539人),中位年龄71.0岁(四分位数间距:68.00~77.00岁),生物学年龄(KDM-BA)中位值71.85岁(67.72~77.19岁),平均KDM-BAA为-0.41岁。非吸烟者占88.62%,非饮酒者占87.56%,中位每周体育锻炼时间90 min,平均BMI(24.65±3.54)kg·m-2,腰围(85.66±9.99)cm。NEU、淋巴细胞(LYM)、PLT中位值分别为3.27×10⁹·L-1、1.62×10⁹·L-1、212.00×1012·L-1,NLR、SII、PLR中位值分别为1.99、424.21、130.99。Fe浓度最高(中位值1233.42 ng·mL-1,几何均数1256.10 ng·mL-1),其次为Cu(中位值891.54 ng·mL-1)。Cu、Zn、Fe、Mn、Se检出率>99%,Cr和Co检出率>75%(原文表1)。
▼原文表1 研究对象基本特征
来源:Journal of Hazardous Materials
2. 微量元素对生物年龄的双向影响
促衰老元素:血清Cu水平每升高1个自然对数单位,KDM-BAA增加2.61岁,呈显著正相关(β=2.61,95%CI:1.29,3.94)(原文图1),且超过临界值(ln Cu>6.5)后加速效应更明显(原文图2)。
抗衰老元素:Zn和Fe则相反,Zn每升高1个自然对数单位,KDM-BAA降低1.57岁(β=-1.57,95%CI:-2.21,-0.94),Fe降低0.65岁(β=-0.65,95%CI;-1.23,-0.06)(原文图1)。
▲原文图1 单个血清ELEs与KDM-BAA之间的关系
来源:Journal of Hazardous Materials
▲原文图2 ELEs与KDM-BAA之间关联的暴露-反应曲线
来源:Journal of Hazardous Materials
联合效应:Qgcomp,WQS和BKMR结果显示,锌、钴、硒、铁的混合物表现出显著抗衰作用,而铜、锰、铬的促衰老效应不显著,提示元素间可能存在拮抗或协同作用,铜的抗衰老效应可能在特定的环境中才能显现(原文图3,图4和图S3)。
▲原文图3 QGC模型结果
来源:Journal of Hazardous Materials
▲原文图4 WQS模型结果
来源:Journal of Hazardous Materials
▲原文图S3 利用BKMR模型研究血清混合ELEs对KDM-BAA的综合影响
来源:Journal of Hazardous Materials
3. 炎症是关键中介通路
生物富集分析:通过在GeneCards和OMIM数据库检索铜,铁,锌和衰老相关靶点,将交集靶点进行GO-BP分析,结果显示,“炎症反应”为核心通路,提示我们“炎症反应”可能是铜铁锌影响衰老的可能通路(原文图5)。
▲原文图5 铜、锌和铁的潜在目标和机制预测
来源:Journal of Hazardous Materials
促炎与抗炎作用:铜升高会显著增加SII、NLR、PLR 等炎症标记物(如SII升高163.76,P<0.05),而锌可降低SII和中性粒细胞计数(SII降低54.04,P<0.05),表明Zn可能通过抗炎效应延缓衰老(原文表2)。
▼原文表2 单一血清ELEs与炎症因子之间的关系
来源:Journal of Hazardous Materials
中介比例:SII、NLR、NEU介导了铜促衰老效8.91%~42.5%,而SII和NEU介导了锌抗衰效应的18.4%~20.0%,证实炎症是微量元素影响生物年龄的核心通路(原文图6)。
▲原文图6 炎症因子对ELEs与KDM-BAA关联的介导效应
来源:Journal of Hazardous Materials
4. 体育运动的调节作用
本研究探讨了PA在微量元素(铜、锌、铁)与炎症及KDM-BAA关系中的调节作用。世界卫生组织建议老年人每周至少进行150 min中等强度体育活动,本研究验证了这一标准对老年人群的适用性。Cu与炎症的交互作用:PA显著调节Cu与炎症标志物(SII、NLR、PLR)的关系(交互作用P值均<0.05)。同时,在不活跃PA组中,Cu与炎症标志物呈显著正相关(βSII=251.18,P<0.001;βNLR=0.84,P<0.001);活跃PA组(≥150 min·周-1)可完全抑制Cu的促炎效应(βSII=64.73,P=0.264)(原文图7)。
▲原文图7 PA在ELEs→炎症→KDM-BAA通路中的调节作用
来源:Journal of Hazardous Materials
Zn的独立作用:PA未显著调节Zn与炎症/KDM-BAA的关联(交互作用P>0.05),提示Zn的抗衰老效应可能独立于PA存在(原文图7)。铁(Fe)的协同效应:高Fe联合不活跃PA与KDM-BAA减少0.78年相关(β=-0.78,P=0.018),达到活跃PA标准可增强Fe的抗衰老作用(高Fe+PA组β=-1.10,P=0.015)(表S6)。机制上PA可能通过促进Fe代谢发挥协同效应。规律PA(≥150 min·周-1)可通过抗炎机制中和Cu的促衰老作用,并与Fe产生协同抗衰老效应,但对Zn介导的衰老调控路径影响有限。研究为老年人群通过PA干预延缓衰老提供了元素特异性指导。
▼原文表S6 血清铁和PA组对KDM-BAA的联合作用
来源:Journal of Hazardous Materials
5. 锌与铜的相互作用
基于Cu和Zn在衰老过程中的拮抗作用,本研究通过分层交互分析探讨了二者的生物学关联。以队列中位数为阈值(Cu:891.54 ng·mL-1;Zn:886.05 ng·mL-1)进行元素分层分析,结果显示:高Zn/低Cu组(Zn>886.05 ng·mL-1且Cu<891.54 ng·mL-1)较参照组(低Zn/低Cu)表现出1.15年的KDM-BAA减缓(β=-1.15,95%CI:-2.00,-0.30;P=0.01),且存在显著相乘交互作用(Pinteraction=0.034)(原文表3)。
Zn/Cu比值生物学意义:Zn/Cu比值与KDM-BAA呈显著负相关(β=-1.97年),提示该比值可能通过双重机制延缓衰老:抑制Cu的促炎效应和增强Zn的抗炎与抗氧化特性,Zn/Cu比值可作为个体化抗衰老干预的潜在生物标志物(原文表3)。
▼原文表3 血清中铜和锌水平对KDM-BAA的联合作用
来源:Journal of Hazardous Materials
研究结论
本研究揭示了微量元素(ELEs)在衰老进程中的差异化作用机制。研究发现,虽然这些元素均参与正常生理功能,但其对KDM-BAA的影响呈现显著差异:Cu在自然对数浓度>6.5时表现出促衰老效应,而Zn和Fe则具有显著抗衰老作用。值得注意的是,Zn的保护效应在低Cu环境下尤为显著,表明元素间存在拮抗作用。机制研究表明,炎症标志物在ELEs与KDM-BAA的关联中起关键中介作用,而PA可通过调控炎症水平有效缓解Cu的促衰老效应。这些发现为基于元素平衡和生活方式干预的衰老防控策略提供了重要理论依据。
河北医科大学公共卫生学院硕士研究生王岩为本文的第一作者。河北医科大学公共卫生学院张荣教授、华中科技大学同济医院荆涛教授和河北医科大学公共卫生学院庞雅贤教授为本文的通信作者。本研究由国家自然科学基金(U24A20772)资助。

北京灵动文化传媒主办联系电话:15101110818邮箱:zuguojizhe@126.com法律顾问:天平法律所
京ICP备20024649号-1京公网安备11010602007323号国家广电许可证编号(京)字第18959号
Copyright © 2024 chinasazh.com. All Rights Reserved本网所刊信息,部分来源于网络,不代表本网观点,如有侵权,请联系删除








